Несколько стран с самыми высокими показателями развития представили, что несмотря на трудность значительного снижения смертности от туберкулеза, его все-таки можно достичь с помощью существующих инструментов и дальнейшего осуществления положительно зарекомендовавших себя интервенций. Чтобы существенно снизить смертность от туберкулеза, мы должны уделять первоочередное внимание предоставлению персонализированных и семейно-ориентированных программ лицам с активной формой туберкулеза, а также охвату населения в группах высокого риска с помощью скрининга и профилактических услуг. Этот комплексный, интегрированный подход требует сначала сосредоточить ресурсы для обеспечения доступности высококачественных услуг по диагностике, лечению и предотвратить все формы туберкулеза как в государственном, так и в частном секторе здравоохранения. Затем необходимо инвестировать в стратегии по выявлению лиц, страдающих туберкулезом в группах высокого риска, и в расширение профилактических мероприятий в этих группах. Хотя для всех стран не приемлем один унифицированный подход, мы выделяем стратегические приоритеты, которые могут служить источником информации при распределении бюджетных средств внутри страны и инвестировании донорами в странах с высоким бременем туберкулеза, и мы также обсуждаем конкретные проблемы, с которыми сталкиваются страны с высоким бременем туберкулеза, где преобладают услуги, предоставляемые частными медицинскими учреждениями, и где распространен или появляется лекарственно-устойчивый туберкулез. Эти рекомендации обобщены в панели 3. Для дополнения эти рекомендаций мы также представляем модельный анализ, проведенный для трех стран с различными эпидемиологическими характеристиками: Кении, Индии и Молдовы
Панель 3: рекомендации Комиссии после совещания ООН высокого уровня по ликвидации туберкулеза
26 сентября 2018 года Комиссия представила дорожную карту, показывающую как страны должны решать свои проблемы с эпидемией туберкулеза. Дорожная карта определяет общие цели стратегии и меры, которые страны могут предпринять для снижения заболеваемости и смертности от туберкулеза.
Расширение стратегий, доказавших свою эффективность
• Убедитесь, что услуги, ориентированные на человека и семью, доступны для всех, кто получает лечение от туберкулеза, гарантируют доступ к качественной диагностике и лечению везде, куда бы они не обращались за помощью
• Охватите группы населения высокого риска, начиная с наиболее легко выявляемых, скринингом, диагностикой и надежной терапией; для охвата этой популяции необходимо участие сообщества и доступность соответствующих ресурсов
• Нацельтесь на определенные группы и людей высокого риска для профилактической терапии вкупе со стратегиями активного выявления случаев заболевания; как только группы высокого риска успешно охвачены, инвестируйте в выявление активных форм туберкулеза среди общего населения, в первую очередь путем укрепления потенциала системы здравоохранения, двигаясь в направлении достижения всеобщего охвата населения услугами здравоохранения
• Отдайте приоритетность взаимодействию с частными поставщиками услуг путем создания партнерства, чтобы улучшить качество медицинской помощи и отчетности о случаях туберкулеза, особенно в странах с высоким бременем туберкулеза с преобладающим частным сектором в сфере оказания медицинской помощи
• Обеспечьте всеобщий доступ к тестированию на лекарственную чувствительность (как минимум к рифампицину) во время постановки диагноза для всех пациентов с туберкулезом, и обеспечьте доступ к тестированию на лекарственную чувствительность к противотуберкулезным препаратам второй линии для всех пациентов с рифампицин-резистентным туберкулезом
Инвестирование в исследования и разработки в области туберкулеза
• Инвестируйте и ускорьте темпы исследований, развития инноваций и разработок в области туберкулеза, включая диагностические, терапевтические и химиопрофилактические стратегии и вакцины, а также популяционных, стратегических, и имплементационных исследований в области народонаселения, политики и внедрения; инвестируйте в исследования по решению проблемы туберкулеза и одновременного заражения ВИЧ, так как туберкулез является ведущей причиной смерти у ВИЧ-инфицированных лиц
• Инвестируйте в оперативные и программные исследования с немедленным внедрением результатов исследований в стратегии борьбы с туберкулезом и программы в области общественного здравоохранения; эти инвестиции представляют собой глобальное общественное благо
• Внедряйте и продвигайте дальше использование существующих биомедицинских инструментов и инструментов профилактики, укрепляйте инфраструктуру и возможности для внедрения новых результатов исследований в программы борьбы с туберкулезом
• Обеспечивайте активную пропаганду в министерствах науки и исследовательских фармацевтических компаниях, в том числе министерствах и компаниях в странах со средним уровнем доходов, чтобы создать глобальную приверженность исследованиям и разработкам в области лечения туберкулеза; финансируйте скорейшее освоение новых продуктов, что послужит важным инвестиционным сигналом для разработчиков продуктов
Обеспечение устойчивого финансирования борьбы с туберкулезом
• Повысьте мобилизацию внутренних ресурсов путем увеличения распределения государственных ресурсов и налоговых поступлений на здравоохранение, объединения финансирования, особенно в странах со средним уровнем доходов
• Уделяйте все больше внимания тому, чтобы донорское финансирование искоренения эпидемии туберкулеза было направлено на инвестирование в глобальные общественные интпресы, в том числе (но не ограничиваясь) в деятельность по формированию рынка, поддержку пропаганды и лидерства, а также исследования и разработки в области борьбы с туберкулезом
• Продолжайте донорское финансирование лечения и профилактики туберкулеза как приоритетной задачи в странах с низким уровнем доходов, а также инвестиции в сокращение распространения, особенно трансграничного распространения лекарственно-устойчивого туберкулеза во всех проблемных странах с низким и средним уровнем доходов
• Разработайте новые модели донорского финансирования, которые стимулируют внутренние инвестиции, поощряйте инновации и усиливайте отчетность перед гражданами, а не перед донорами
Создание благоприятной среды для борьбы с туберкулезом
• Ускорьте прогресс в направлении всеобщего охвата населения услугами здравоохранения; в странах с высоким бременем туберкулеза особенно важно внедрение устойчивых НТП, которые отдают приоритет помощи и профилактике туберкулеза на пути к достижению всеобщего охвата населения услугами здравоохранения
• Усиливайте лидерство и участие гражданского общества во всех аспектах разработки противотуберкулезных программ путем укрепления и повышения их роли в принятии решений в политике, реализации и подотчетности, а также инвестирование в их участие как в глобальное общественное благо
• Установите механизмы независимой, многоотраслевой отчетности, в том числе создание подборок данных, чтобы обеспечить ответственность всех заинтересованных сторон, особенно правительств и их партнеров по развитию, за прогресс в направлении ликвидации эпидемии туберкулеза.
Обеспечение доступа к качественным персонализированным медицинских услугам
Определение персонализированной помощи
Для принятия эффективных мер в отношении лиц с туберкулезом и уменьшения задержек в диагностике, терапии и излечении, медицинские услуги, оказываемые пациентам с туберкулезом, должны быть ориентированы на человека, то есть быть целостными, индивидуализированными, обеспечивающими расширение их прав и возможностей, основанными на уважении и поощряющими принятие обоснованных решений и свободное волеизъявление114. Учитывая, что туберкулез обычно влияет на семьи, и члены семьи людей с туберкулезом подвержены высокому риску развития туберкулеза, услуги должны быть ориентированы также на семью115 в дополнение к персонализированному подходу. Таким образом, тщательная оценка моделей поведения лиц, нуждающихся в медицинских услугах, эпидемиологии туберкулеза, а также данных местной демографической ситуации и системы здравоохранения необходимы для определения приоритетных ресурсов и первоочерёдности решения проблем обеспечения медицинской помощи116. Обеспечение всеобщего доступа к высококачественной, персонализированной помощи при туберкулезе лицам, уже получающим медицинскую помощь, в любых условиях должно быть главным приоритетом.
К сожалению, во многих странах с высоким бременем туберкулеза недостатки системы здравоохранения препятствуют оказанию персонализированной противотуберкулезной помощи: часто люди с туберкулезом не выявлены или их состояние не оценено своевременно117,118; и даже после постановки диагноза не начато вовремя лечение или не контролируется его соблюдение, что препятствует завершению лечения и полному стойкому исцелению. Медицинские услуги, оказываемые пациентам с туберкулезом, должны соответствовать моделям поведения лиц, нуждающихся в этих услугах для обеспечения персонализированной помощи и профилактики. Оптимизация согласования услуг, оказываемых как в НТП, так и в негосударственном секторе (например, частными поставщиками медицинских услуг, неправительственными организациями), может помочь обеспечить более высокие показатели излечения туберкулеза и повысить эффективность оказания медицинской помощи, чтобы обеспечить равенство и контроль расходов. Устраняя неравенство в доступности и повышении эффективности оказания услуг и обеспечивая защиту пациентов с физическими и финансовыми трудностями, эти вмешательства также являются неотъемлемой частью устойчивых систем здравоохранения и более широкой повестки дня ООН по ЦУР119.
Переосмысление механизма предоставления услуг по лечению туберкулеза
Как показала декларация совещания ООН высокого уровня по ликвидации туберкулеза, политические обязательства по продвижению политики, ориентированной на человека, сильны, равно как и твердые этические и моральные обоснования для принятия персонализированного подхода к лечению туберкулеза. Предоставление пациентам права выбора места, где можно получить помощь, и предоставление им права взятия под свою ответственность медицинских решений может иметь благоприятные последствия для здоровья, как это было показано в России. В одном исследовании в Томске, России120, где злоупотребление алкоголем является основной сопутствующей патологией для МЛУ-ТБ, лицам, выпавшим из дальнейшего наблюдения медицинскими работниками, были предложены меры по снижению потребления алкоголя и нормализации рациона питания, транспортная поддержка, а также право выбора места, где они хотели бы получать постоянную медицинскую помощь (стационар, дневной стационар или на дому). После проведения данного вмешательства, соблюдение схем лечения улучшилось с 52% до 81%, и в 71% случаев был достигнут успех лечения.
Чтобы достигнуть успеха, принцип персонализированной помощи при туберкулезе требует радикального переосмысления того, как будет предоставляться лечение. К сожалению, многие НТП не спешили внедрять новые модели оказания помощи, так как были ограничены небольшими техническими возможностями, скудными ресурсами и множеством конкурирующих приоритетов. Данная Комиссия подчеркивает, что противотуберкулезные программы должны постоянно развиваться, реагировать на изменение демографических факторов, предпочтений пациентов и доступных данных. Предоставление дифференцированных услуг, оказываемых ВИЧ-инфицированным пациентам показало не только, как инновации в предоставлении услуг могут повысить эффективность и результативность, а также как сообщества могут формировать и информировать системы. Аналогичные стратегии необходимы для трансформации службы оказания противотуберкулезной помощи. Заметные различия в отдельных демографических группах, таких как пожилые люди (> 65 лет) и мужчины трудоспособного возраста, показывают, что единая универсальная стратегия, основанная на принципе «один размер подходит всем» не состоятельна. Не вызывает сомнения необходимость реализации адаптивных моделей персонализированной помощи, которые могут снизить заболеваемость туберкулезом в течение жизни одного поколения114.
Согласование противотуберкулезной помощи с моделями обращения за помощью
Чтобы реализовать концепцию устойчивого здоровья для всех, мы должны обеспечить, чтобы системы здравоохранения были полностью обеспечены ресурсами, чтобы все лица с риском туберкулеза могли получить доступ к диагностическим, лечебным и профилактические услугам. Нужны немедленные и дополнительные действия, чтобы гарантировать, что имеющиеся ресурсы распределены соответствующим образом с долгосрочной целью создания оптимально интегрированной, персонализированной системы здравоохранения. Для достижения этих целей программы по борьбе с туберкулезом должны так направить ресурсы, чтобы они соответствовали тому, куда и как люди с туберкулезом и те, кто подвержен риску развития болезни, могли обратиться за помощью. Анализ пути пациента (PPA), картирующий непрерывную цепочку оказания помощи пациентам с туберкулезом, использование существующих популяционных исследований и обычных программных данных могут позволить программам улучшить их понимание того, насколько хорошо можно скоординировать обращения за медицинской помощью с доступностью услуг по лечению туберкулеза, и обозначить системные барьеры для доступности медицинской помощи для пациентов. Этот шаг важен для расстановки приоритетов и планирования услуг для удовлетворения потребностей и предпочтений пациентов. Данный метод хорошо изучен 121, и в 2017 году были опубликованы результаты внедрения PPA в пяти странах и поэтапную модель оказания медицинской помощи в двух других странах19. Этот анализ показал заметные несоответствия между возможностями диагностики туберкулеза и моделями поведения лиц, нуждающихся в медицинских услугах, когда менее 30% учреждений, в которых пациенты могут начать лечение, имеют возможности сделать микроскопию мазка мокроты и еще меньшее количество — сделать тест GeneXpert или обеспечить направление образца для тестирования GeneXpert20. Эти результаты также указывают на необходимость в приоритетном порядке наладить проведение быстрых молекулярных тестов в одних определенных местах и механизмы направления биологических образцов в других. Кроме того, PPA показал важность данных на уровне медицинского учреждения для обеспечения эффективности, целевого распределения ресурсов и улучшения сети ПМСП, чтобы найти упущенные случаи туберкулеза.
В 2016 году стратегическая и техническая консультативная группа ВОЗ по туберкулезу рекомендовала всем странам завершить PPA как часть установления приоритетов и процессов планирования122. Было опубликовано руководство по внедрению, однако только менее десяти стран имеют завершенные субнациональные PPA или поэтапные модели оказания медицинской помощи121.
Надежная, ориентированная на человека расстановка приоритетов и планирование требуют изменений в том, как сопоставляются и переводятся данные. Множество требований к сбору данных часто исходят от НТП с многочисленными разобщенными точками данных, их слишком много, и ими трудно оперировать при принятии решений. Более того, в большинстве мест при планировании мероприятий, в основном, использовались эпидемиологические данные для информирования при распределении ресурсов, а не то, как и куда должны быть направлены ресурсы, чтобы удовлетворить предпочтения пациента. Несколько недавних исследований улучшило наше понимание моделей обращения за медицинской помощью и возможностей системы здравоохранения, тем не менее, немногие из этих данных регулярно включаются в процессы планирования. К сожалению, получение достоверных данных в значительной степени определялось планированием сверху вниз, а не ключевыми программными вопросами от НТП. В дополнение, запросы доноров о научно-обоснованных планах не согласованы и не синхронизированы с процессами планирования на страновом уровне. Как следствие, страны могут быть зациклены на процессе вечного планирования, не имея времени на реализацию и обучение, что делает процесс консолидации надежных данных для каждого плана практически невозможным.
Разработка персонализированных программ требует, чтобы данные и доказательства были консолидированы для идентификации пробелов в непрерывной цепочке оказания медицинской помощи. Это также требует, чтобы излечившиеся от туберкулеза и их представители играли неотъемлемую роль в разработке, реализации и оценке программ лечения туберкулеза. Систематический и бескомпромиссный персонализированный подход к использованию этих данных (см. приложение) позволяет НТП предпринять шаги, необходимые для преодоления препятствий, мешающих лицам с туберкулезом получать медицинские услуги, быть диагностированными даже при посещении медицинского учреждения, быть информированными или получать и завершить лечение.
Чтобы поддерживать страны в продвижении к персонализированному планированию, необходимо будет лучше увязать глобальную архитектуру туберкулеза, включая надзор, техническую помощь и финансирование от доноров, с этим поэтапным персонализированным подходом. Глобальные результаты программы по туберкулезу не контролируют ликвидацию пробелов вдоль пути пациента или в конкретных медицинских вмешательствах, оптимизированных для пациента. Для решения этой проблемы, PPA должны систематически проводиться как ключевые компоненты пакета доказательств и служить информационной основой для расстановки приоритетов и помощи доноров. Хотя из этого следует, что перераспределение ресурсов на модели поведения, направленные на обращение за медицинской помощью, должно повысить эффективность выделения ресурсов НТП, для подтверждения этого предположения необходимы дальнейшие исследования.
Использование оптимизации сети и анализ больших данных для обеспечения всех пациентов доступом к услугам
Оптимизация сети — это одна из стратегий, которую можно использовать в странах с высоким бременем туберкулеза для обеспечения того, чтобы пациенты с симптомами туберкулеза, многие из которых выпадают из пути пациента на этапе диагностики39, имели доступ к быстрым и точным диагностическим услугам. Заимствуя аналитические подходы из производственных отраслей, оптимизация сети стремится решить, как обеспечить выбор лучшей ее конфигурации из доступных альтернатив на основе выбранных критериев. Применимо к службам диагностики туберкулеза это может помочь сбалансировать необходимость расширения доступа к диагностическим услугам для наиболее нуждающихся в них при обеспечении экономической эффективности и целесообразности, размещения инструментов информирования, транспортировки образцов, реферальных механизмов, кадрового обеспечения и географической расстановки приоритетов. Более того, путем интеграции данных из других диагностических инструментов (например, рентгенографии грудной клетки и тестирования на ВИЧ) и программ по другим заболеваниям (например, услуг по уходу и лечению ВИЧ-инфицированных) оптимизация сети может позволить более точное распределение ресурсов по секторам и программам здравоохранения. Одним из примеров такого подхода является Лесото, где диагностическое сетевое картирование использовалось для анализа тестирования и поэтапной модели оказания помощи в рамках НТП, и информированного решения о закупках. Несмотря на высокую неудовлетворенную потребность и наличие GeneXpert тестирования, в 19 из 25 учреждений использовалось менее половины возможностей его проведения. Первоначально НТП планировала закупить и развернуть дополнительные инструменты в сети, однако анализ показал, что пропускная способность сети может быть лучше оптимизирована за счет улучшения реферальных потоков и корректирования того, куда лучше разместить существующие инструменты. Анализ также определил оптимальные места, которые в соответствии со спросом пациентов целесообразно оснастить средствами точечной диагностики. Анализ привел к рекомендациям о перераспределении для максимального эффекта 62% инструментов GeneXpert тестирования в стране. Для улучшения эффективного использования инструментов GeneXpert также были скорректированы реферальные потоки внутри и за пределами районов, что предотвратило необходимость приобретать дополнительные инструменты.
В ближайшем будущем большие данные, агрегированные из рутинных отчетов министерств здравоохранения, операционных планов донорских агентств, данных частного сектора здравоохранения и социальных сетей, равно как и других секторов правительства помогут преобразовать эффективность программ по туберкулезу, позволяющих целевое расширение услуг и предоставляющих небывалую прежде информированность о положении дел и аналитические возможности для министров здравоохранения и управленцев НТП. В настоящее время в условиях ограничения ресурсов мы наблюдаем мало примеров агрегирования данных, используемого для улучшения доступности персонализированных программ. Тем не менее, платформы интегрированных данных в сочетании с технологией моделирования, позволяют НТП создавать подробные модели случаев туберкулеза в реальном времени, включающие разнообразие моделей поведения, направленного на обращение за медицинской помощью, диагностических возможностей, расходах на медицинскую помощь. В будущем такие системы данных могут обеспечить удобные панели управления на каждом уровне системы здравоохранения, с единым интерфейсом для статического анализа сложных систем и их анализа в реальном времени, позволят НТП прогнозировать изменения спроса пациентов, ожидаемого дефицита, контролировать использование диагностических и лечебных средств и, в конечном счете, улучшить обслуживание пациентов. Использование источников агрегированных, больших данных потребует специализированного оборудования, стандартов совместимости, последовательного сбора данных и систем анализа, а также регулирующего надзора.123 Однако эти подходы уже успешно применяются в решении и других сложных проблем системы здравоохранения в США124,125 и в других местах126. Конечно, такие нововведения могут успешно помочь устранить пробелы в доступности противотуберкулезных программ, особенно если они используются в тандеме с технологиями, расширяющими возможности пациентов. Например, прорывная возможность смартфонов увеличить формирование спроса на услуги, повысить ответственность поставщиков127 и оптимизировать приверженность128, 129 является весьма существенной130. Эффект этих цифровых решений, вероятно, будет постепенным и неоднородным, преувеличенным в короткий срок, но недооцененным до конца в долгосрочной перспективе123.
Улучшение управления качеством для обеспечения оказания услуг высокого качества
Чтобы обеспечить доступ к услугам для всех пациентов с туберкулезом в дополнение к PPA и анализу конструкции сети, мы должны улучшить качество медицинской помощи, которую получают пациенты. К сожалению, анализ поэтапных механизмов оказания помощи показывает большие различия в качестве медицинской помощи как и для взрослых и детей, так и для лекарственно-чувствительного туберкулеза, и для лекарственно-устойчивого туберкулез во многих странах с высоким бременем туберкулеза35–37,111,131. Симуляционные исследования пациентов в Индии, Кении, Южной Африке и Китае33, 34, 45 показали низкое качество медицинской помощи, оказываемой пациентам с туберкулезом35. В исследовании в Китае, например, поставщики медицинских услуг в 59% случаев неправильно вели пациентов с типичными симптомами и с признаками активного туберкулеза34. В индийском исследовании только одна треть практикующих врачей правильно вели пациентов с туберкулезом даже при наличии симуляционного учебника по этому заболеванию32.
Традиционно программные эффекты и результаты измерялись в первую очередь эпидемиологическими критериями. Такой фокус, однако, упускает из виду, что результаты, связанные с улучшением качества помощи за счет устранения пробелов в поэтапной модели оказания помощи, более актуальны в оперативном отношении и могут ускорить прогресс. Инструменты управления качеством могут помочь передовым поставщикам услуг и управленцам НТП устранить эти пробелы, чтобы улучшить качество медицинской помощи, а также заняться основными факторами постоянного распространения инфекции.
Программы управления качеством должны стать частью НТП и в идеале интегрироваться в существующие национальные программы управления качеством (см. приложение). Чтобы обеспечить это, руководители НТП и их команды, имеющие такие знания и опыт, должны способствовать разработке способов оценки и улучшения качества. Тем не менее, изменения механизмов использования данных о туберкулезе для улучшения качества медицинской помощи должны происходить на каждом уровне системы здравоохранения, включая повышение ответственности местных противотуберкулезных диспансеров перед пациентами, которых они обслуживают. Глобально программа управления качеством, которая включает методы улучшения, может стать мощным рычагом для усовершенствования подотчетности доноров и получателей и повысить эффективность деятельности доноров. ВОЗ играет решающую роль в поддержке программы управления качеством и создании глобальной культуры, которая обеспечивает улучшение качества и ускоряет распространение обучения через взаимный обмен. Связь донорской поддержки с качественными показателями может также повысить эффективность донорского финансирования и его прозрачность.
Улучшение качества: уроки, извлеченные из программ по борьбе с ВИЧ
За последние несколько десятилетий программы по борьбе с ВИЧ в страны Африки к югу от Сахары, Карибского бассейна и Азии внедрили программы управления качеством для оптимизации использования ограниченных ресурсов, полученных от правительств и донорских агентств133. Основные элементы управления качеством включают официальный план управления качеством, техническую рабочую группу или комитет, набор показателей эффективности, ожидаемые результаты реализации деятельности по улучшению качества, наращивание потенциала персонала и участие пациентов и/или сообщества. Эти элементы необходимы, чтобы добиться устойчивости в случае ожидаемой текучки персонала и изменений окружающей среды, которые влияют на стабильность организаций здравоохранения и кадров. Используя четырехступенчатый непрерывный цикл улучшения (по принципу «Планируй-делай-проверяй-действуй»), эти программы влекут за собой существенные изменения путем разработки местных решений для улучшения качества медицинской помощи при ВИЧ. Эти улучшения были показаны в различных аспектах помощи, включая приверженность лечению134, сокращение передачи ВИЧ от матери ребенку135, педиатрические услуги136, более строгое соблюдение руководящих принципов лечения137 и усиление клинических возможностей передовых поставщиков услуг138.
Подобные подходы могут быть использованы и для улучшения качества помощи пациентам с туберкулезом, а также для повышения ответственности на всех уровнях НТП (тематические исследования в приложении показывают примеры из государственного и частного сектора того, как подходы к улучшению качества на уровне медицинского учреждения и на региональном уровне были направлены на улучшение результатов программ по туберкулезу).
Используя модели поэтапного оказания медицинской помощи в качестве организационной структуры, НТП могут измерять качество на уровне медицинского учреждения при помощи набора показателей, которые представляют собой ключевые шаги в осуществлении поэтапной помощи или которые отражают международные стандарты медицинской помощи, оказываемой при туберкулезе (см. приложение) 139. Национальная отчетность по этим показателям качества может помочь НТП выявлять малоэффективные объекты здравоохранения, которые требуют дополнительной поддержки или ресурсов. Кроме того, медицинские учреждения могут использовать инструменты по анализу коренных причин для определения конкретных барьеров и разработки идей для их решения.
Однако, как было отмечено Комиссией журнала Lancet по вопросам глобального здравоохранения при рассмотрении аспектов качества систем здравоохранения 26 улучшение качества потребует общесистемных действий, выходящих за рамки усилий по улучшению качества только в отдельно взятом медицинском учреждении. Эти действия включают более эффективное управление качеством; внедрение медицинского образования на основе требований к компетентности и обучения этике и уважительному отношению; создание среди населения спроса на качество для наделения людей полномочиями и расширенными правами, чтобы они могли держать систему подотчетной и активно обращались за высококачественной медицинской помощью.
Оценка эффективности стратегий для обеспечения персонализированных медицинских услуг высокого качества
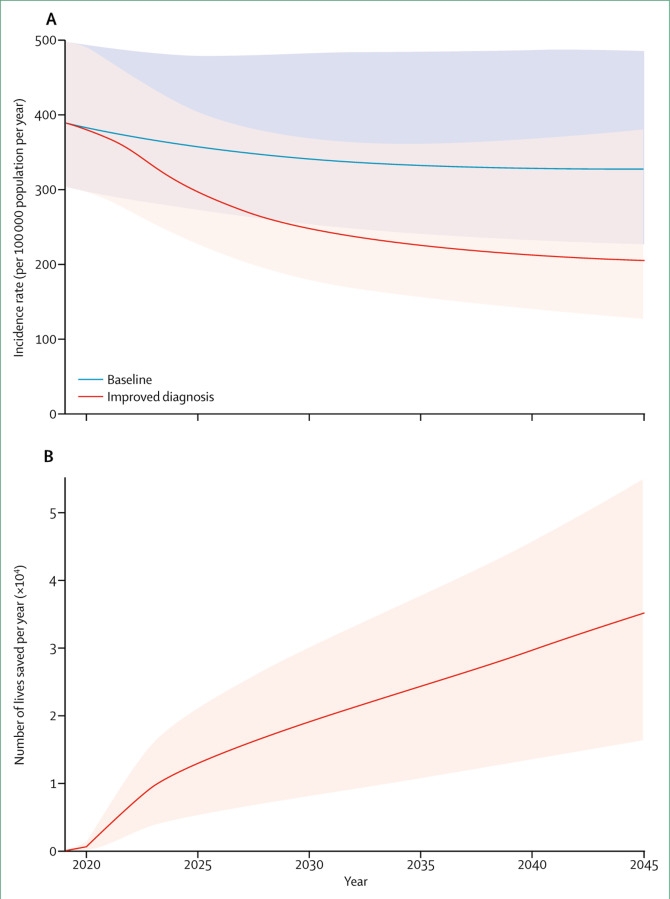
Все стратегии, описанные в этом разделе, разделяют общую цель как можно ранней точной диагностики туберкулеза: они отражают способы реализации максимального потенциального эффекта от системы услуг, оказываемых пациентам с туберкулезом, которые зависят от представленных случаев, требующих помощи. Модельный анализ, проведенный Весга и соавт.140 специально для этого отчета в сотрудничестве с Комиссией, дает некоторое представление о потенциальной ценности этих и других мер в трех разных странах, имеющих свои определенные проблемы в борьбе с туберкулезом: Индия (с большим частным сектором поставщиков услуг), Кения (с ВИЧ-инфекцией) и Молдова (с высоким бременем лекарственно-устойчивого туберкулеза). Пример Кении показан на рисунке 3: в этом случае РРА уже определил в качестве ключевой проблемы нехватку диагностических средств21. На рисунке показан потенциальный эффект мер, которые могут увеличить вероятность постановки диагноза за одно посещение поставщика медицинских услуг до 90%: эффект заключается в уменьшении кумулятивных случаев заболевания туберкулезом в 2018-2045 гг. на 25% (95%-ный достоверный интервал 11–39), а кумулятивной смертности за тот же период — на 36% (95%-ный достоверный интервал 17–50). Как описано в этом разделе, такие меры не ограничиваются диагностическими инструментами: они также задействуют оптимизацию сети, исправляя несоответствие медицинской помощи при туберкулезе и других мер для эффективного использования методов быстрой и точной диагностики. Как показало моделирование, эти меры необходимы, но недостаточны, чтобы положить конец пандемии туберкулеза. Тем не менее, в сотрудничестве с другими стратегиями, изложенными в разделе 1, они могут помочь странам добиться существенного прогресса в деле прекращения эпидемии туберкулеза.
Рисунок 3. Показатели заболеваемости и спасенных жизней в Кении в результате улучшенной диагностики туберкулеза
Показатель заболеваемости (на 100 000 населения в год)
Базовый
После улучшенной диагностики
Число спасенных жизней в год (× 104)
|
Снижение
показателя (% [95% достоверный интервал])
в 2018-2045 гг.
|
Кумулятивное
снижение в 2018-2045 гг.:
| ||
|
Количество(x105
[95% достоверный интервал])
|
%
(95% достоверный интервал])
| ||
|
Случаи
туберкулеза
|
15,8
(4–26)
|
17,4
(7,2–19,6)
|
25
(11–39)
|
|
Смертность
от туберкулеза
|
20,7
(8–32)
|
5,4
(2,3–8,5)
|
36
(17–50)
|
(A) Показатель заболеваемости туберкулезом (на 100 000 населения в год)
(B) Показатель спасенных жизней (на 100 000 населения в год).
Синяя линия соответствует базовому сценарию, где все условия остаются неизменными, тогда как красная линия показывает результаты сценария вмешательства с повышенной до 95% вероятностью точного диагноза в течение одного визита врача пациентом. Подробные методы, используемые для моделирования этих сценариев, описаны Весга и соавт.140.
Приоритетность активного выявления случаев заболевания туберкулезом
Помимо целевого использования ресурсов и проведения анализа для обеспечения пациентов с туберкулезом персонализированной помощью высокого качества, другой приоритетной задачей является активное выявление людей с туберкулезом, особенно среди групп высокого риска, которые еще не получили помощи. Стратегии по выявлению этих выпавших из внимания пациентов должны выполняться вместе с расширением доступа к профилактическим вмешательствам. Эти две стратегии — активное выявление и профилактика — должны быть в программном отношении неразделимы, как и не разделены в отношении распределения бюджета. Хотя активное выявление случаев туберкулезом в основном касается раннего выявления и своевременного лечения лиц с активным туберкулезом, тем самым снижая смертность, заболеваемость, расходы пациентов и постоянное распространение, оно также направлено на выявление и лечение лиц с латентной формой туберкулезной инфекции141.
Активное выявление случаев: сокращение пробелов между теорией и практикой
Исследования распространенности туберкулеза в странах с высоким бременем болезни142–144 предоставляют многочисленные доказательства того, что, несмотря на увеличение и децентрализацию диагностики и лечения туберкулеза, невыявленные случаи остаются важной проблемой, особенно для групп высокого риска145–148. К сожалению, в большинстве стран с высоким бременем туберкулеза недостаточно широко внедрены стратегии по выявлению этих лиц из-за нехватки финансирования, политической воли и научного консенсуса149–151. Как результат, влияние стратегий активного выявления случаев туберкулеза на эпидемиологию туберкулеза в условиях высокого бремени болезни ограничено; были опубликованы неоднозначные результаты лишь нескольких исследований150–153. Тем не менее, имеющиеся клинические исследования154, математическое моделирование155,156 и значительный программный опыт156,157 предполагают, что эти стратегии могут быть широко внедрены. В России в 2015 году почти половина бремени туберкулеза была выявлена путем активного скрининга 68% лиц, находящихся в местах лишения свободы. В Бразилии скрининг заключенных на туберкулез, проведенный в 2015 году, выявил 6021 новых случаев — 8% всего национального бремени туберкулеза158.
Хотя для реализации стратегии активного выявления случаев необходим системный подход, министерства здравоохранения и их партнеры также должны рассмотреть вопрос о том, как расширить мероприятия по целевому выявлению случаев. Важные аспекты этой проблемы включают постановку четких целей и задач на основе тщательной оценки ситуации; выявление и приоритизацию групп риска; выбор простых алгоритмов и точных, эффективных технологий157,159. Кроме того, следует рассмотреть возможность использования передового опыта для распространения инноваций116,160; установить и использовать сети взаимодействий для изменений; активно вовлекать сообщество; и обеспечить сильное руководство и управление, чтобы гарантировать успех деятельности по активному выявлению случаев. Связывание этих стратегий со структурой подотчетности и финансирования, основанных на удовлетворении поставленных целей, также может сыграть свою положительную роль.
Приоритетность групп высокого риска
Несколько групп населения с заболеваниями или воздействиями, которые ставят их в группу высокого риска развития туберкулеза, всегда должны систематически обследоваться (см. приложение). Бытовые контакты этих лиц всегда должны быть приоритетными для скрининговых программ, учитывая силу доказательств, показывающих эффект стратегий, нацеленных на них161. Семейно-ориентированный подход и признание того, что туберкулез — это болезнь, которая поражает семьи, имеют важное влияние на активное выявление случаев заболевания, поэтому НТП должны рассматривать семью, а не одного человека в качестве единицы вмешательства.
Другие группы риска могут требовать целевых скрининговых программ на основе эпидемиологии, возможностей системы здравоохранения, доступности ресурсов и их осуществимости. Учитывая более высокую заболеваемость туберкулезом среди мужчин по сравнению с женщинами почти во всех группах высокого риска13, дружественные к мужчинам стратегии, такие как мероприятия на рабочем месте, должны использоваться везде, где это возможно. При подготовке расширения стратегии активного выявления случаев заболевания необходимо тщательно рассмотреть риск дискриминации и стигматизации. Также необходимо учитывать правовой статус мигрантов в отношении как доступа к медицинским услугам, так и риска экспатриации в случае выявления туберкулеза162. Для улучшения понимания проблем и ожиданий групп высокого риска во время планирования и проведения скрининга на туберкулез для их успеха имеет решающее значение вовлечение гражданского общества.
Возможности интеграции стратегии активного выявления случаев туберкулеза с другими важными услугами для этих групп населения должны использоваться при каждом удобном случае, особенно когда группы высокого риска уже обслуживаются вертикальными программами на базе отдельных учреждений163 или частными поставщиками медицинских услуг164 , или когда мероприятия по активному выявлению случаев туберкулеза могут быть увязаны с другими мероприятиями по укреплению здоровья165. Для некоторых групп высокого риска, таких как люди, живущие в трущобах, и бездомные, может быть необходимо применение инновационных, многоплановых стратегий, использующих технологии здравоохранения, и включение стратегий социальной защиты чтобы максимально увеличить доходность и рационализировать расходы164,166.
Одного активного выявления случаев будет недостаточно для искоренения туберкулеза в группах высокого риска. Даже если переместить больше людей с туберкулезом в группы риска, они снова вернутся в свои прежние группы высокого риска, где распространенность факторов риска туберкулеза высока. Многосекторальный подход имеет важное значение для обеспечения того, чтобы были устранены такие факторы риска туберкулеза, как недоедание и загрязнение воздуха. Также важно, чтобы мероприятия по активному выявлению случаев были неотделимы от вмешательств, направленных на предотвращение туберкулеза у латентно-инфицированных и более высокого риска развития активной болезни.
Прогнозирование затрат и использование инструментов планирования
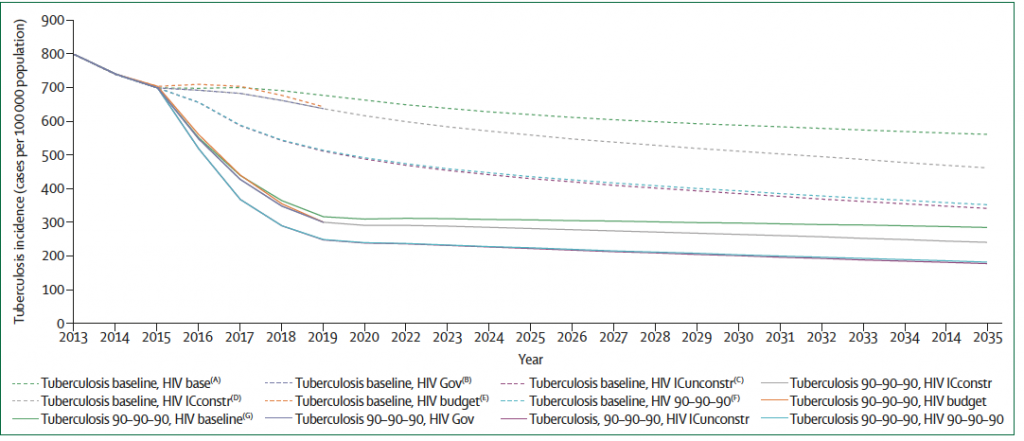
Для расширения стратегий активного выявления случаев туберкулеза потребуются значительные дополнительные ресурсы. Стоимость скрининга может быть высокой для каждого выявленного случая167–169, особенно по сравнению с другими мероприятиями по укреплению здоровья170. Тем не менее, доказательства экономической эффективности и преимуществ расширенного финансирования для активного выявления случаев туберкулеза предполагают, что такие инвестиции принесут высокую отдачу. Моделирование, проведенное в рамках инвестиционного планирования программы по туберкулезу правительством Южной Африки (рисунок 4), показывает, что снижение распространения туберкулезной инфекции в результате высокого уровня выявления случаев заболевания и оптимального лечения будет иметь высокую экономическую эффективность, если будет достигнуто значительное и длительное снижение заболеваемости и распространенности туберкулеза. Другие моделирующие исследования, которые включают изучение выгод от снижения распространённости, также подтверждают, что даже при высокой стоимости скрининга стратегии активного выявления случаев туберкулеза могут быть очень рентабельными155,169.
Инструменты планирования, такие как он-лайн инструмент ВОЗ ScreenTB172 может помочь НТП в планировании их деятельности по выявлению случаев и определении приоритетности групп риска для скрининга путем моделирования потенциального выхода скрининга и затрат на различные скрининговые подходы. Инструмент ScreenTB позволяет пользователю выбирать группы риска и сравнивать оценки результативности и выхода скрининга (в том числе количество выявленных истинно-положительных и ложноположительных случаев), общих затрат, стоимость одного выявленного случая относительно выбранной группы риска и различных алгоритмов скрининга.
Рисунок 4: Пример инвестиционного планирования программы по туберкулезу в Южной Африке
Заболеваемость туберкулезом (число случаев на 100 000 населения)
ТБ – баз.сцен., ВИЧ — баз.сцен (A)
ТБ – баз.сцен., ВИЧ — ICconstr (D)
ТБ – 90-90-90., ВИЧ — баз.сцен (G)
ТБ – баз.сцен., ВИЧ — Gov (B)
ТБ – баз.сцен., ВИЧ – бюджет. (E)
ТБ – 90-90-90., ВИЧ — Gov
ТБ – баз.сцен., ВИЧ — ICunconstr (C)
ТБ – баз.сцен., ВИЧ – 90-90-90. (F)
ТБ – 90-90-90., ВИЧ — ICunconstr
ТБ – 90-90-90., ВИЧ — ICconstr
ТБ – 90-90-90., ВИЧ — бюджет
ТБ – 90-90-90., ВИЧ — 90-90-90
(A) Базовый сценарий (т.е. традиционный подход к финансированию).
(B) Цели правительства (Gov): текущее сочетание мероприятий по борьбе с ВИЧ и туберкулезом в течение следующих 5 лет с текущими целями охвата, утвержденными правительством.
(C) Сценарий оптимизации без ограничений (ICunconstr; т.е. наиболее эффективное сочетание мер против ВИЧ и туберкулеза без бюджетных ограничений).
(D) Сценарий оптимизации с бюджетными ограничениями (ICconstr; т.е. результаты оцениваются с использованием текущего бюджетного пакета).
(E) Бюджетный сценарий 90–90–90, который был адаптирован для сценария в соответствии с бюджетом.
(F) Оптимизация в отношении целей 90-90-90. Наиболее экономически эффективный пакет мероприятий для достижения целей 90-90-90.
(G) Сценарий 90–90–90, нацеленный на выявление и лечение 90% случаев туберкулеза к 2020 году,
с достижением успеха в лечении у 90% из тех, кто получает терапию.
Воспроизводится с разрешения Министра здравоохранения Южной Африки.171
Использование технологий для повышения эффективности стратегии выявления случаев туберкулеза
При определении эффективности систематического скрининга решающее значение имеют инструменты, используемые для скрининга и диагностики туберкулеза. Медицинская сортировка по системе Триаж, которая позволяет проводить активный скрининг в сообществах, была бы более эффективным, персонализированным подходом к выявлению случаев, чем доступные подходы, и требует значительных инвестиций (см. приложение). Мобильные автоматические цифровые рентгенографические аппараты для обнаружения поражения легких у людей при относительно бессимптомном течении болезни173,174 могут также помочь выявить гораздо больше пациентов с туберкулезом, чем это возможно при пассивном выявлении или самообращении. Хотя данные об этом редки175, компьютеризированные инструменты обнаружения, используемые совместно с цифровой рентгенографией, могут существенно повысить диагностическую чувствительность, а также сэкономить средства. Очевидно, что эта технология также повысит чувствительность для выявления других патологий, в дополнение к туберкулезу легких, подчеркивая важность включения активного выявления случаев в условиях комплексной ПМСП.
В дополнение к новым диагностическим технологиям улучшение использования доступных данных, агрегированных и анонимных, собранных из различных источников, в том числе социальных сетей, аптек46 и частного сектора, могут повысить точность и эффективность мероприятий по активному выявлению случаев заболевания, а также обеспечить распространение данной стратегии от групп высокого риска до сообществ с низким уровнем риска. В Уганде уже был опыт объединения данных социальных сетей, записей мобильных телефонов и пространственных данных для увеличения масштабов тестирования на ВИЧ176, а также в городских центрах Кении, чтобы показать, что завезенная малярия существенно способствует бремени болезни177. Следует заметить, что использование этих дополнительных данных будет незначительно влиять на осуществление мероприятий по активному выявлению случаев туберкулеза, если только они не будут интегрированы в существующие системы данных.
Выявление случаев туберкулеза в группах низкого риска
Охват всего населения мероприятиями по активному выявлению случаев туберкулеза должен оставаться низким приоритетом до тех пор, пока не будет успешно охвачена вся популяция высокого риска. Тем не менее, признавая, что активное выявление случаев является вмешательством высокой значимости как с эпидемиологической, так и экономической точки зрения, в странах с высоким бременем туберкулеза не должны быть проигнорированы и группы населения с низким уровнем риска. Определение наиболее эффективного сочетания вмешательств и стратегий, которые НТП могут использовать для выявления пациентов как с высоким, так и с низким уровнем риска, а также расширение прав и возможностей руководителей НТП для выбора наиболее подходящей комбинации подходов для их уникальных условий являются ключом к успеху. Внутри страны разные провинции или районы могут использовать различные методы, в зависимости от социально-демографических характеристик населения, участия гражданского общества и активов системы здравоохранения. Выбор соответствующих мер вмешательств и стратегий основывается на строгом, непрерывном процессе научных исследований, обмена знаниями, мониторинге и оценке.
Приоритетная профилактика туберкулеза
Профилактика туберкулеза является крайне важной, но зачастую ею пренебрегают как компонентом глобального контроля эпидемии заболевания. За последние 50 лет стратегии борьбы с туберкулезом в странах с высоким бременем туберкулеза сосредоточились на пассивном выявление случаев и лечении активного заболевания, несмотря на многочисленные политические рекомендации, пропагандирующие повышенное внимание к вмешательствам по выявлению случаев156,157,178,179. Математическое моделирование показывает, что нацеленность лишь на пассивные стратегии, хоть и предотвращают смертельные случаи и уменьшают заболеваемость, однако не смогут ликвидировать туберкулез. Искоренение туберкулеза потребует использования нескольких различных профилактических вмешательств, чтобы прервать распространение инфекции, лечить латентные формы, вакцинировать контакты больных, а также лечить или предотвращать сопутствующие заболевания, такие как ВИЧ, которые повышают восприимчивость к развитию активного заболевания. Таблица 4 показывает некоторые группы населения, которым профилактические вмешательства принесли бы немало преимуществ183. Борьба с туберкулезной инфекцией в учреждениях здравоохранения и местах коллективного проживания (например, тюрьмы) также имеют решающее значение для проведения профилактических мероприятий: медицинские центры и больницы часто являются очагами распространения туберкулеза, и введение контроля окружающих условий и строгих административных и индивидуальных защитных мер может существенно снизить риск распространения инфекции.
Таблица 4. Группы населения, получающие выгоды от профилактической терапии туберкулеза, и ответственность за доступ к профилактическим мероприятиям в системе здравоохранения
| Риск прогрессирования | Данные по миру | Ответственные за выполнение |
Ссылка
| |
|
Пациенты
с ВИЧ-инфекцией
| 2–10% в год | ~ 30 млн. человек | Национальные программы по СПИДу |
ЮНЭЙДС(UNAIDS)180
|
| <5 контактов домохозяйств | 5–40% за 2 года |
~
5,5 млн. человек
в
год
|
ПМСП,
программы по туберкулезу,
программы
охраны здоровья матери и ребенка
|
Dodd
и соавт.
181
(2014)
|
| > 5 контактов с домохозяйствами | До 10% за 2 года |
~
20 млн. человек
в
год
|
ПМСП,
НТП
|
Fox
и соавт.
150
(2018);
Morrison
и соавт.
182 (2008)
|
| Медицинские работники в местах с тяжелым бременем ТБ | 1–3% в год, переменная | > 10 млн. человек | Национальные и местные системы здравоохранения | — |
| Заключенные в местах с тяжелым бременем ТБ | 1–10% в год | > 10 млн. человек | Исправительные учреждения | — |
Целевая профилактическая терапия
Профилактическая терапия туберкулеза, вероятно, предлагает одно из наиболее эффективных вмешательств для снижения заболеваемость туберкулеза во всем мире. Кроме того, через профилактику туберкулеза и снижение смертности путем лечения пациентов с латентной инфекцией, которые имеют наибольший риск развития активного заболевания, профилактическая терапия туберкулеза является необходимым компонентом комплексной стратегии для прекращения пандемии. Даже улучшенные стратегии диагностики и лечения не могут охватить значительного количества латентно инфицированных людей (приблизительно 2 миллиарда. человек), которые могут заболеть туберкулезом в любой момент в их жизни56. Четко нацеленная профилактическая терапия туберкулеза может существенно снизить заболеваемость туберкулезом в группах повышенного риска. Эти группы включают людей с ВИЧ; бытовые и прочие тесные контакты людей с инфекционным туберкулезом; людей, работающих или живущих в условиях, способствующих распространению микобактерий туберкулеза, таких как места коллективного проживания, тюрьмы, медицинские учреждения185, 186 и подземные шахты, особенно те рабочих, которые подвергаются воздействию кремнезема, что само по себе значительно увеличивает риск развития болезни147,187. Более того, сам процесс предоставления профилактической терапии туберкулеза выявляет активные случаи заболевания, так как кандидаты на профилактическую терапию проходят скрининг, чтобы исключить заболевание перед началом лечения, которое и обнаруживает ранее не выявленные случаи туберкулеза.
Хотя эффективность профилактической терапии для предупреждения активного туберкулеза хорошо известна59, в программах общественного здравоохранения приоритетное внимание больше уделяется выявлению случаев туберкулеза и лечению, чем реализации этого недорогого и высокоэффективного вмешательства. Программы борьбы ВИЧ были сосредоточены в основном на проведении жизненно важной антиретровирусной терапии, не в последнюю очередь из-за убедительных доказательств ее эффективности в качестве вмешательства для профилактики туберкулеза188,189. Исследования показали, что профилактика туберкулеза с использованием изониазида существенно снижает смертность у людей как на ранней, так и на поздней стадии ВИЧ-инфекции190-192. Моделирующие исследования свидетельствуют, что широкое внедрение профилактической терапии туберкулеза в сочетании с улучшением выявления случаев заболевания и лечения важнее эффективных вакцин для достижения ликвидации туберкулеза к 2050 г. 192, и, что изучение контактов домохозяйств и использование этой терапии предотвратила бы 99000–117000 смертей в год среди детей младше 15 лет193. Эти данные подчеркивают важность семейно-ориентированного подхода к оказанию медицинской помощи при туберкулезе для того, чтобы обеспечить, чтобы все эти контакты регулярно проходили скрининг как часть планового ведения всех лиц с диагностированным туберкулезом.
Многочисленные препятствия мешают расширению масштабов профилактической терапии, и для их преодоления необходимо применить инновационные подходы183. Усовершенствованные диагностические тесты для регистрации туберкулезной инфекции, включая тестирование на местах, будет способствовать лечению инфекции у лиц с повышенным риском развития туберкулеза, таких как домашние контакты, хотя контактировавшие дети младше 5 лет и все ВИЧ-инфицированные лица, живущие в местах с высоким бременем туберкулеза теоретически могут проходить терапию и без тестирования. Прогностические биомаркеры, идентифицирующие лиц со скрытой инфекцией, которая чаще всего прогрессирует до активной болезни, позволит более целенаправленное использование профилактической терапии в группах высокого риска и более широкое ее использование в группах низкого риска. Глобальные поставки основных лекарств, таких как изониазид, и более новых препаратов, таких как рифапентин, являются ненадежными, также часто наблюдается их нехватка; следовательно, улучшение цепочки поставок недорогих препаратов гарантированного качества имеет решающее значение. Курс профилактической терапии с использованием изониазида, продолжающийся 6-9 месяцев, часто приводит к несоблюдению лечения и распространению широкой обеспокоенности, в основном необоснованной194, о профилактической терапии, вызывающей устойчивость. Новые краткосрочные схемы лечения, такие как 12-недельная терапия еженедельного приема рифапентина и изониазида или 4-недельный режим каждодневного приема рифапентина и изониазида, могут изменить профилактические мероприятия175–177 и снизить риск возникновения лекарственной устойчивости, в то же время экономя средства и спасая жизни195,198,199. Тем не менее, вместо того, чтобы ждать новых диагностических методик и более кратких курсов лечения, данная Комиссия утверждает, что НТП должны расширить доступ к профилактической терапии уже сейчас и мы видим примеры того, как НТП и их партнеры успешно внедрили профилактическую терапию туберкулеза в широких масштабах (см. приложение).
Для реализации полного эффекта профилактической терапии НТП должны обеспечивать ресурсы, чтобы гарантировать интеграцию мероприятий по активному выявлению случаев заболевания и профилактической терапии в существующие программы для определенных групп риска. Интеграция скрининга на туберкулез и профилактических услуг в медицинскую помощь для ВИЧ-инфицированных лиц крайне важна, особенно учитывая результаты обширного, высококачественного исследования, показавшего преимущества этой стратегии, позволяющей спасти жизни190, 200. Глобальные усилия по предоставлению антиретровирусной терапии позволили охватить 20 миллионов ВИЧ-инфицированных людей, но еще 17-19 миллионов их остаются без лечения. Менее 4 миллионов человек с ВИЧ когда-либо получали противотуберкулезную профилактическую терапию, показывая возможность существенно расширить это вмешательство. Отсутствие расширения масштабов этой терапии для людей, живущих с ВИЧ, вероятно, стало причиной нескольких миллионов смертей в прошлом десятилетии200.
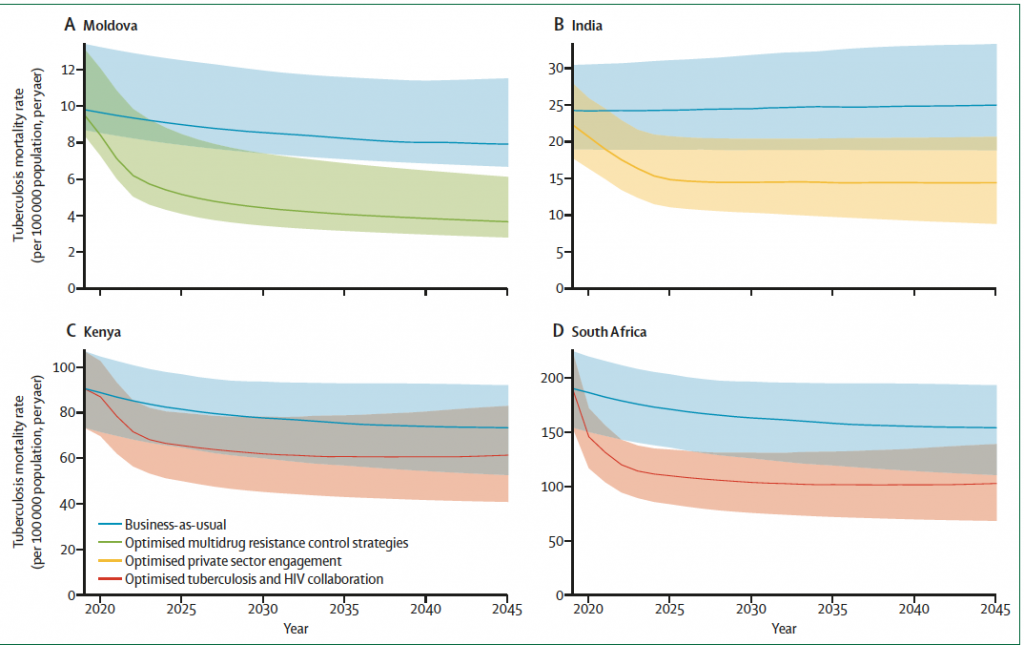
Анализ, проведенный Весга и соавт, был направлен на определение эффекта противотуберкулезной профилактической терапии с использованием изониазида, как это рекомендовано для стран с высокими показателями распространённости туберкулеза с попутным инфицированием ВИЧ. При увеличении охвата противотуберкулезной профилактической терапией ВИЧ-инфицированных лиц в Кении до 90% (рисунок 5), смертность от туберкулеза может быть снижена на 17% в период между 2020 и 2045 гг . В ЮАР аналогичное увеличение охвата лечением приведет к еще большему сокращению показателей смертности за тот же период времени. Чтобы достичь этого эффекта, а также распространить профилактическую терапию для других соответствующих групп населения, рекомендованных ВОЗ201, потребуются дополнительные инвестиции. Дополнительные затраты на программу расширения профилактической терапии туберкулеза в Кении и ЮАР будут относительно невысокими (66 млн. долларов США в год в период между 2018 и 2045 гг.. для достижения результатов, выделенных на рисунке 5), особенно по сравнению с экономическими издержками предотвратимых случаев смерти в результате невыполнения этой стратегии. Эффективность этих инвестиций может быть усилена оптимальным использованием данных систем здравоохранения для содействия НТП и их партнерам в планировании вмешательств и мониторинге эффективности профилактических стратегий202, 203. Подборки данных по туберкулезу, отслеживающие прогресс этих данных на региональном и местном уровнях, могут также помочь ускорить расширение масштабов профилактической терапии туберкулеза и гарантировать, чтобы НТП и их партнеры были больше подотчетны организациям гражданского общества и спонсорам. Успех усилий по осуществлению масштабной профилактической терапии туберкулеза также будет зависеть от признания важности совместной ответственности всех программ здравоохранения и заинтересованных сторон.
Рисунок 5: Жизни, потенциально спасенные от туберкулеза в разных странах
Коэффициент смертности от туберкулеза (на 100 000 населения, в год)
Коэффициент смертности от туберкулеза (на 100 000 населения, в год)
A Молдова
В Индия
C Кения
D ЮАР
Традиционный подход
Оптимизированные стратегии контроля множественной лекарственной устойчивости
Оптимизированное участие частного сектора
Оптимизированное сотрудничество программ по туберкулезу и ВИЧ
Показаны прогнозы смертности при различных сценариях вмешательств, специфичных для каждой из
четырех стран с высоким бременем ТБ
(А) Потенциальный эффект улучшения контроля множественной лекарственной устойчивости
в Молдове, S с высоким бременем МЛУ-ТБ. Повышение раннего тестирования лекарственной чувствительности до 90% всех диагностированных случаев туберкулеза и увеличение успешности лечения новыми схемами препаратами второго ряда до 85% позволит снизить заболеваемость МЛУ- ТБ на 73% (95% достоверный интервал 66–80) в 2045 г. по сравнению с 2015 г. и предотвратит 43% (34–51) случаев смерти от туберкулеза.
(B) Потенциальный эффект от привлечения частного сектора в Индии при условии сбора данных из 90% частных поставщиков услуг по лечению туберкулеза и оптимизации данного вида медицинских услуг. Предполагается, что уровень оказания медицинской помощи пациентам с ТБ в частном секторе в Индии поднимется до уровня государственного сектора здравоохранения путем сочетания субсидирования диагностики ТБ и механизмов поддержки приверженности лечению. Эти меры позволят предотвратить 21% случаев смертей от ТБ (95% достоверный интервал 17–34) между 2018 и 2045 гг..; в этот период они будут связаны со средними дополнительными затратами в размере 290 млн. долларов США в год (85–645).
без учета затрат на лечение лекарственно-устойчивого туберкулеза.
(C) Потенциальный эффект от улучшения сотрудничества между программами по ВИЧ и туберкулезу в Кении и (D) в ЮАР. Представлены прогнозы смертности в этих двух сценариях с высоким бременем ВИЧ-инфекции в сопоставимых условиях в Кении и ЮАР, где доля людей с одновременным заражением ТБ и ВИЧ составляет 16% и 60%, соответственно. В обоих случаях увеличение охвата антиретровирусной терапией до 90% по сравнению с текущим уровнем и увеличение охвата профилактической терапией изониазидом среди лиц, проходящих лечение от ВИЧ, до 90% по сравнению с текущим уровнем, приведет к снижению смертности на 33% (95% достоверный интервал 18–49) в условиях, аналогичных Кении, и на 46% (30–62) в условиях, аналогичных ЮАР. На примере Кении эти меры будут включать средние дополнительные затраты в размере 66 млн. долл. США в год (95% достоверный интервал 20–113) в период между 2018 и 2045 гг. Смета расходов не включает расходы на лечение лекарственно-устойчивых форм ТБ. Включение этих расходов, вероятно, приведет к снижению дополнительных затрат вследствие снижения бремени МЛУ-ТБ.
Важность участия частных поставщиков медицинских услуг: от признания до установления приоритетов
В большинстве стран с низким и средним уровнем доходов, частные поставщики медицинских услуг являются важным источником медицинской помощи для людей всех социально-экономических групп, часто предлагая доступность и удобство, не предусмотренные в государственной системе. Строго говоря, «частный» — синоним «негосударственного» и включает в себя как учреждения, получающие прибыль, так и некоммерческий сектор (т.е. НПО и религиозные организации). Хотя большинство стран смогли улучшить участие поставщиков услуг из государственного, некоммерческого и религиозного секторов, сложность представляет привлечение коммерческих частных поставщиков услуг, хотя они являются более важными игроками в борьбе с туберкулезом. В этом разделе мы обсудим некоторые причины неудач в привлечении частных поставщиков медицинских услуг, рекомендации того, как они могут быть масштабно задействованы в оказании противотуберкулезной помощи, и важнейшие действия стран, которые они должны принять, чтобы вовлечение частных поставщиков услуг стало приоритетом в рамках страновых программ по туберкулезу. Мы обращаем внимание на стратегии обеспечения качественной противотуберкулезной помощи в частном секторе, возможности для большего взаимодействия между НТП и частными поставщиками, и на то, как можно использовать расширенные возможности, которые обеспечивает частный сектор, чтобы выявить людей с туберкулезом, упущенных усилиями по надзору в рамках этих программ.
Привлечение частных поставщиков медицинских услуг должно стать приоритетом
Необходимость привлечения частных поставщиковдляконтроля туберкулеза была признана в различных глобальных стратегиях с начала 1990-х годов204. К сожалению, НТП и их партнеры по развитию были недостаточно сосредоточены на привлечении частных поставщиков противотуберкулезной помощи, а имеющихся ресурсов было недостаточно, чтобы реально заняться решением этого вопроса. До выделения средств в 2009 году Глобальный фонд для борьбы со СПИДом, туберкулезом и малярией, который обеспечивает 56% международной помощи в целях развития программ по туберкулезу, выделил чуть меньше 5% грантового бюджета для привлечения целого ряда поставщиков ненациональных противотуберкулезных программ, что было обозначено как государственно-частное партнерство205. Так как Глобальный фонд отвечает на запросы стран о том, как будут использоваться их грантовые средства, в конечном итоге этот небольшой процент бюджета отражает тот низкий приоритет, который страны придают взаимодействию с частными поставщиками. Хотя данные о том, сколько национальные программы тратят на привлечение частных поставщиков скудны, пример из Индии показателен: до 2009 года только 1,5% государственных расходов на туберкулез было выделено для привлечения НПО и частных провайдеров услуг206.
Плохое взаимодействие с частными поставщиками услуг часто приписывается дефициту кадров НТП, но очевидно, что корни проблемы лежат гораздо глубже207. Большинство систем здравоохранения в странах с низким и среднем уровнем доходов слабы в вопросах, которые необходимы для эффективного привлечения частных поставщиков услуг, например, таких как выполнение нормативных требований, стратегические закупки, информационные системы здравоохранения. Национальные программы часто имеют недостаточную базовую информацию о количестве частных поставщиков, их роли в обращении больных туберкулезом за помощью и основных факторах поведения в схеме «пациент-поставщик». Поэтому менеджерам национальных программ трудно привлечь сотни и тысячи независимых частных провайдеров с различными возможностями. Со своей стороны, частные поставщики услуг часто опасаются участвовать в государственных программах и, учитывая динамику конкурентного рынка и финансовые обязательства, не желают придерживаться руководящих принципов национальных программ.
Неспособность осмысленно вовлекать частных провайдеров отражает сильные предпочтения в отношении государственного сектора тех, кто управляет противотуберкулезными программами, тех, кто выделяет на них средства, и тех, кто оказывает техническую поддержку в привлечении в выполнение этих программ. Сообщество по борьбе с туберкулезом успешно внедряет множество инноваций, в том числе новые методы диагностики, инструменты лечения и подходы для борьбы с туберкулезом и коинфекцией ВИЧ, а также с МЛУ-ТБ. Эти инновации, однако, могут быть приняты и в частном секторе, не оспаривая основные бизнес-модели государственного сектора. Усилия по вовлечению частных поставщиков могут добиться масштабных успехов только тогда, когда НТП признают, что они не могут продолжать дальнейшую деятельность на основе существующей бизнес-модели (таблица 5). Тем не менее, такое взаимодействие должно происходить одновременно со стратегиями, защищающими пациентов и их семьи от серьезных финансовых потерь, которые могут возникнуть в результате обращения за медицинской помощью в частный сектор208, 209. В работе по прекращению эпидемии туберкулеза в странах с большим частным сектором будет важно защищать интересы людей, живущих в бедности, гарантируя, что государственные ресурсы применяются для снижения финансовых затрат пользователей при одновременном использовании частного сектора для расширения диагностического и лечебного охвата.
Таблица 5: Вовлечение частных поставщиков медицинских услуг как прорывнаяинновация для НТП
| Доступная операционная модель |
Прорывная
операционная модель
| |
| Скрытая миссия и роль | Помощь, оказываемая больным туберкулезом, которые обращаются за ней в государственные учреждения; выступать в качестве поставщика услуг | Помощь всеми больным туберкулезом независимо от того, куда они обращаются; выступать в качестве посредника оказания услуг |
| Согласование предоставления услуг | Государственные провайдеры и учреждения, быстро реагирующие на направления НТП | Все поставщики и учреждения, расставленные по приоритетам в соответствии с предпочтениями пациента |
|
Подход
к частным поставщикам и
рынкам
оказания медицинских услуг
|
Конкурировать
и не доверять частным поставщикам;
отрицать или бороться с рыночными
силами
| Сотрудничать и наладить партнерство с частными поставщиками, о чем свидетельствует их роль в рыночной системе здравоохранения; признавать и использовать рыночные силы |
| Ментальная карта для взаимодействия | Предпочтение в стандартизации; нисходящие, основанные на политике инновации; линейные системы | Комфорт с неопределенностью и адаптацией; инновации как развивающиеся эволюционные процессы; сложные адаптивные системы |
| Инструменты для взаимодействия | В основном внутренние: формы, стандартизированные процедуры и инструкции |
В
основном внешние: стимулы, вспомогательные
средства и контракты.
|
| Основные навыки и компетенции | Линейное управление, контроль и логистика |
Переговоры,
влияние и закупки
|
| Основные навыки и компетенции | Персонал и руководство медицинским персоналом | Персонал и руководство со знаниями и опытом, в т.ч. по социальным наукам, системам здравоохранения и финансов в здравоохранении |
| Данные для принятия решений | В подавляющем большинстве медицинские данные: сервисная статистика по уведомлениям о случаях и результатах лечения; слабые или непоследовательные данные об источнике уведомлений и передаче случаев; нет данных о распределении ресурсов по типу поставщиков | Баланс медицинских и социально-экономических данных, в том числе: цифры, характеристики, локализация и услуги по туберкулезу, оказываемые всеми видами поставщиков; пути обращения пациентов за помощью их предпочтения; поведение и мотивация поставщиков; объемы и тенденции продаж частными поставщиками; распределение ресурсов по типу поставщиков |
| Финансирование для привлечения частных поставщиков | Краткосрочное, имеющие разовый характер, в небольших объемах, внешнее; дополнительно сверх панируемого, урезается и сокращается в первую очередь | Интегрировано в основные бюджеты; долгосрочное; в крупных масштабах; внутреннее и внешнее |
| Условия финансирования | Основанные на затратах, связанные с предложением, за предыдущие периоды |
Основанные
на результативности, часто связанные
со спросом
|
Ускорение прогресса и новые возможности для взаимодействия с частными поставщиками
Хотя участия частного сектора в борьбе с туберкулезом далеко недостаточно, накоплен значительный опыт относительно того, как успешно привлечь частных поставщиков медицинских услуг210. За несколько последних лет было реализовано много небольших, поддерживаемых извне пилотных проектов, привлекших частных провайдеров. Исследование 2006 года изучило результаты 15 проектов в восьми странах 211, систематический обзор в 2011 году рассмотрел 45 исследований из 22 проектов в 12 странах212, и еще одно исследование в 2016 году ознакомилось с 78 исследованиями, предоставляющими информацию о 48 программах в 16 странах213. Большинство проектов не достигли значительного масштаба или не смогли остаться устойчивыми в течение длительного периода. Тем не менее, эти проекты породили многочисленные доказательства того, что привлечение частных провайдеров может существенно увеличить выявление случаев туберкулеза и достичь показателей успеха лечения, которые, по крайней мере, ничуть не хуже результатов, достигаемых в государственном секторе. Также доступны, хотя и менее достоверны, данные об экономической эффективности, финансовой защите, несвоевременном лечении и охвате малоимущих214. Новые исследования продолжают способствовать более глубокому пониманию функционирования рынков частной системы здравоохранения в отношении туберкулеза33, 215, 216.
С 2012 года устойчивое расширение взаимодействия с частными поставщиками медицинских услуг имело место в нескольких ключевых странах (рисунок 6). В Бангладеше с 2012 года наблюдалось умеренное привлечение частных поставщиков медицинских услуг, с заявлением об охвате частным сектором 18% случаев заболевания в 2016 году, в то время как сообщалось, что в Мьянме за аналогичный период времени этот показатель снизился по сравнению с такими же цифрами 2012 года. Индия, Пакистан и Филиппины увеличили участие частных провайдеров с уведомлениями от них об охвате частным сектором до 9 -13% случаев заболевания в 2016 году. К сожалению, в Индонезии и Нигерии, двух странах со значительным количеством упущенных больных туберкулезом, достигнут незначительный прогресс, с уведомлениями согласно оценкам в среднем о 4% для Индонезии и 1% для Нигерии. \
В Бангладеше, Мьянме и Пакистане участие большого количества частных поставщиков первичной медицинской помощи было возглавлено сильными НПО, выступившими посредниками между поставщиками услуг и НТП. Эти управляемые своей миссией НПО определили участие частного сектора в борьбе с туберкулезом в рамках их долгосрочной роли и преуспели в привлечении ресурсов от множества доноров для поддержания их работы. Некоторые организации являются универсальными НПО, такие как Бангладешский комитет по сельскому развитию и Корпус милосердия в Пакистане; другие больше сосредоточены на туберкулезе, такие как Фонд Дэмиена в Бангладеше и Интерактивные исследования и разработки в Пакистане; Гринстар в Пакистане и Международная организация по обслуживанию населения в Мьянме являются организациями социального маркетинга, которые давно находятся на частном рынке, занимаясь вопросами планирования семьи и другими вопросами здравоохранения. Все эти организации в целом имеют понимание деятельности частных провайдеров, умение осуществлять масштабную деятельность, сильные системы управления (в области человеческих ресурсов, информации и логистики), динамичное руководство, способность к адаптации и инновациям и успехи в сборе средств.
Рисунок 6: Процент пациентов с туберкулезом, о которых уведомили частные поставщики медицинских услуг, среди общего числа пациентов с туберкулезом с 2012 по 2016 гг. в семи странах с высоким бременем туберкулеза с преобладающей частной системой здравоохранения
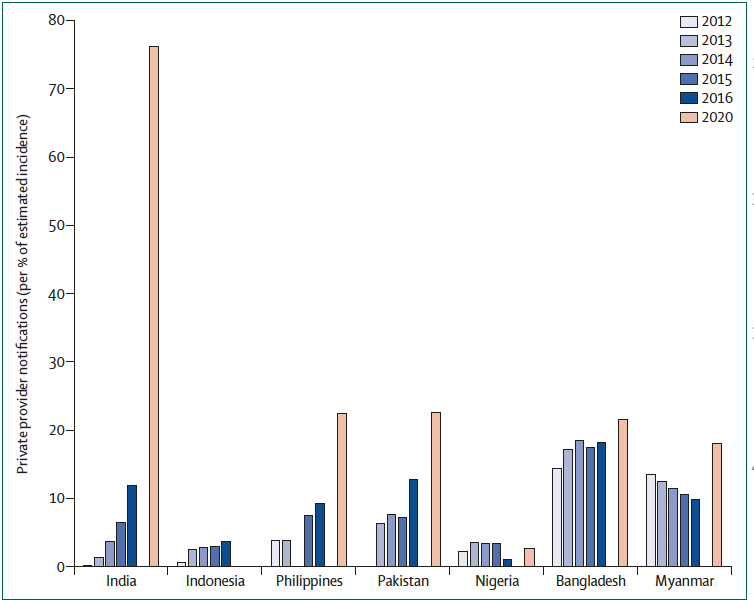
Этот процент представлен в качестве целевого показателя на 2020 год для Бангладеш, Индии, Мьянмы, Нигерии, Филиппин и Пакистана (где данные были доступны в НТП).
Уведомления частных поставщиков (в % от предполагаемой заболеваемости)
Индия Индонезия Филиппины Пакистан Нигерия Бангладеш Мьянма
Усилия в Индонезии и на Филиппинах были больше сосредоточены на частных специалистах и больницах, а не на поставщиках ПМСП. НТП сотрудничали со специализированными ассоциациями (например, Индонезийским обществом пульмонологов и Филиппинским обществом по туберкулезу). Тем не менее, большая часть первоначальной помощи и лечения туберкулеза в этих странах осуществляется частными поставщиками ПМСП и, следовательно, потребуются дополнительные усилия для привлечения этих поставщиков. Схемы социального медицинского страхования, приближающиеся к полному охвату населения в обеих странах, предусматривают заключение контрактов с растущим количеством частных провайдеров услуг ПМСП. Тем не менее сотрудничество между национальными программами и социальным медицинским страхованием остается весьма ограниченным16.
Одним из самых захватывающих событий является взятие политических обязательств в 2017 году в Индии по расширению взаимодействия с частным сектором по всей стране, которое опирается на успех нескольких крупных демонстрационных проектов (см. приложение)17. Национальный стратегический план Индии по туберкулезу (на 2017–2020 годы) заявляет о наращивании сотрудничества с частными поставщиками медицинских услуг и призывает к шестикратному увеличению уведомлений от них до 2 миллионов пациентов в год к 2020 году, что составляет 75% от предполагаемой заболеваемости туберкулезом. Если этот план будет успешно осуществлён, то Индия будет первой крупной страной с высоким бременем туберкулеза с доминирующим частным сектором здравоохранения, в которой деятельность программ по туберкулезу скоординирована с моделями оказания помощи населению. Цели по уведомлениям от частного сектора о случаях заболеваний туберкулезом в Бангладеше, Пакистане и Филиппинах гораздо скромнее: 18–24% от предполагаемой заболеваемости туберкулезом к 2020 году (рисунок 6). В целом, по крайней мере, десять стран недавно подготовили портфель продуктов с планами действий по управлению18, и последний раунд финансирования от Глобального фонда для борьбы со СПИДом, туберкулезом и малярией на 2018–2020 гг. включает существенный компонент для вовлечения частных поставщиков медицинских услуг в нескольких странах.
В качестве успешного доказательства участия частных провайдеров сообщается, что определенные пакеты вмешательств могут быть распространены в виде шаблонов, которые могут быть адаптированы для быстрого оперативного реплецирования опыта19. Основные вмешательства в таких шаблонах включают определенные мероприятия для привлечения частных поставщиков (например, консультации с заинтересованными сторонами, картирование поставщиков и расстановка приоритетов, управление отношениями, содействие отчетности о случаях и данных о туберкулезе, а также поддержка приверженности пациента); рассмотрение вопросов финансового и нефинансового стимулирования частных провайдеров; и обеспечение того, чтобы пациенты частных учреждений имели доступ к высококачественным лекарствам и диагностике в соответствии с национальными протоколами. Хотя интервенционные пакеты могут и были обобщены в общий вид, следует поощрять постоянные инновации и их адаптацию.
Кроме того, необходимо создать нормативно-правовую базу, чтобы обеспечить уведомления о случаях болезни и качественные услуги от частных провайдеров медицинских услуг. Несколько стран переиздали законы и правила, требующие от поставщиков сообщать о случаях заболевания, иногда регулирующие повторное лицензирование и аккредитацию на уведомления о туберкулезе20. Хотя регулирующие санкции могут сыграть свою роль, страны, наиболее успешные в привлечении частных провайдеров, больше инвестировали в средства поддержки (например, колл-центры для содействия уведомлениям) и стимулы (такие как легкий доступ к лекарствам и диагностике), при этом уважая интересы провайдеров. Профессиональные общества могут быть и были успешно вовлечены, чтобы помочь определить лучшие практики и описать передовой опыт по борьбе с туберкулезом среди частных поставщиков медицинских услуг.
Забегая вперед, новые возможности и разработки могут повысить заинтересованность частного поставщика услуг в борьбе с туберкулезом в ближайшие годы. Во-первых, успех в такой стране, как Индия, может показать пример, который вдохновляет другие страны. Во-вторых, цифровая революция, наконец, достигла мероприятий по борьбе с туберкулезом: использование информационных и коммуникационных технологий (ИКТ) в сочетании с колл-центрами, может способствовать привлечению частных провайдеров и предоставлять цифровую информацию о пациентах с туберкулезом, проходящих лечение в частном секторе, в НТП или специалистам по туберкулезу. В-третьих, такие ИКТ системы могут обеспечить дополнительные инновации, которые в дальнейшем будут способствовать привлечению частных поставщиков медицинских услуг, такие как применение цифровых ваучеров на лекарства и диагностические средства, соблюдение технологии мониторинга и цифровой оплаты, льготы и дополнительные возможности как для пациентов, так и для поставщиков услуг. В-четвертых, доступ к новым и улучшенным диагностическим методикам и инструментам для лечения, таким как цифровая рентгенография грудной клетки и GeneXpert MTB/RIF, увеличил ценность для частных провайдеров и взаимодействие с государственным сектором. Наконец, появление схемы социального медицинского страхования с целью всеобщего охвата населения услугами здравоохранения предлагает беспрецедентную платформу для широкомасштабного привлечения частных провайдеров при любом состоянии здоровья и обеспечивает возможность улучшить качество и доступ как лечебных, так и профилактических услуг по лечению туберкулеза в частном секторе ПМСП в таких странах, как Индонезия и Филиппины217. Серьезно обстоит дело с оптимизацией частного сектора с целью обеспечения высокого качества лечения туберкулеза, в то же время защищая пациентов от чрезмерных личных затрат. Чтобы быть успешными эти модели должны минимизировать платежи за платные услуги, которые вознаграждают количество вместо качества и не поощряют недорогие вмешательства высокой ценности, такие как профилактика туберкулеза. Тем не менее, как часть более широкой повестки дня относительно всеобщего охвата услугами здравоохранения, использование услуг частного сектора для предоставления финансируемых государством услуг может позволить широкие возможности при одновременном учете предпочтений лиц, наиболее подверженных туберкулезу или больных туберкулезом218.
Моделирование результатов оптимального вовлечения частного сектора
Из-за большого бремени туберкулеза, проблемой которого во всем мире занимается и частный сектор, важно оценить эффект от улучшения взаимодействия с ним. Моделирование, выполненное для данного отчета оценивало, насколько более активное участие частного сектора в странах с тяжелым бременем болезни, например, в Индии, где частные провайдеры предлагают расширенные возможности, может повлиять на заболеваемость и смертность от туберкулеза. В подобных условиях стратегии по улучшению качества помощи, оказываемой частными поставщиками медицинских услуг, такие как субсидирование диагностики туберкулеза и механизмы поддержки пациентов частных медицинских учреждений по соблюдению схем лечения, финансируемые национальными программами, предотвратят 28% смертей от туберкулеза в течение следующих 30 лет, спасая еще 8 миллионов жизней, не считая жизней, спасенных в результате полной реализации других научно-обоснованных мер (рисунок 5). Оптимизация вовлечения частного сектора будет стоить дополнительно 290 млн. доллпров США ежегодно. Хотя реализации только одной этой стратегии будет недостаточно, чтобы положить конец эпидемии в Индии, у нее есть достаточный потенциал, чтобы существенно уменьшить угрозу для общественного здравоохранения, вызываемую туберкулезом. Дальнейшее улучшенное участие частного сектора в сочетании с другими стратегиями для устранения пробелов в поэтапной модели оказания помощи, такими как целенаправленные меры по активному выявлению случаев, оптимизация диагностических сетей и улучшение поддержки приверженности к лечению, может привести к существенному сокращению смертности от туберкулеза в течение следующих 30 лет219.
Борьба с лекарственной устойчивостью
Прогнозы показывают, что в течение следующего десятилетия, по крайней мере, у 6 миллионов человек разовьется лекарственно-устойчивый туберкулез. Без улучшений в предоставлении лечения и успешности терапии лекарственно-устойчивого туберкулеза, большинство людей с этой формой туберкулеза умрут, при этом распространяя ее дальше. Ожидается, что к 2050 году ведущей причиной четверти из прогнозируемых 10 миллионов ежегодных смертей в мире, связанных с устойчивостью к противомикробным препаратам, станет именно лекарственно-устойчивый туберкулез, и M.tuberculosis — наиболее серьезный возбудитель, передаваемый воздушно-капельным путем, устойчивый к лекарствам220.
Учитывая эти прогнозы, решение проблемы резистентности к противотуберкулезным препаратам важно как для решения глобальной проблемы устойчивости к противомикробным препаратам, так и для ликвидации туберкулеза. Хотя обеспечение всеобщего тестирования на лекарственную устойчивость и расширение доступа к высококачественному, специализированному лечению лекарственно-устойчивого туберкулеза потребует значительного финансирования и обязательств, последствия игнорирования этих мер могут быть чудовищными, включая огромные человеческие жертвы и триллионы долларов, потраченных в будущем на проблему значительного роста распространенности туберкулеза с множественной лекарственной устойчивостью220. Более того, решение проблемы лекарственной устойчивости туберкулеза не может быть отделено от расширения доступа к диагностике и лечению лекарственно-чувствительного туберкулеза; если мы улучшим выявление случаев лекарственно-чувствительного туберкулеза без существенного изменения качества выявления лекарственно-устойчивого туберкулеза мы будем только способствовать избирательность в борьбе с данным заболеванием.
Анализ моделирования, выполненный для данного отчета, демонстрирует эффект обеспечения всеобщего доступа к терапии лекарственно-устойчивого туберкулеза и терапии препаратами второго ряда в странах с высокой распространенностью лекарственно-устойчивого туберкулеза, таких как Молдова. Как показано на рисунке 5, оптимизация доступа к лекарственно-устойчивому туберкулезу и улучшение показателей успешности лечения приведет к сокращению смертности от туберкулеза на 43% и снижению заболеваемости на 73% в течение следующих 30 лет. При адекватных инвестициях в необходимые инструменты перспектива окончательного устранения угрозы лекарственно-устойчивого туберкулеза в течение жизни одного поколения заслуживает доверия.
Отрадно, что быстро развивающаяся область диагностики и увеличение доступности новых и перепрофилированных используемых препаратов и схем лечения пациентов с МЛУ-ТБ или с устойчивостью к рифампицину предоставляет возможность резко улучшить ответ эпидемии (см. приложение). Вновь появляющиеся данные предполагают, что в условиях высокой нагрузки более 90% случаев МЛУ-ТБ или туберкулеза с устойчивостью к рифампицину являются результатом прямой передачи уже устойчивых бактерий туберкулеза между людьми72,73. Как результат, отсутствие диагностирования и неэффективное лечение значительной части людей с активным заболеванием являются основной движущей силой эпидемии. Барьеры для диагностики и расширения масштабов лечения варьируются в зависимости от страны, но включают высокую стоимость лечения (хотя данные показывают, что расходы могут значительно уменьшиться, если обеспечить доступ к диагностике и лечению большему количеству людей)221; кажущуюся сложность схем лечения; скудные результаты программного лечения большей частью из-за длительных и токсичных схем терапии, наносящих большой вред здоровью; зависимость от централизованного и специализированного лечения; и отсутствие политической воли и обязательств222–225.
Поскольку большинство лекарственно-устойчивых форм туберкулеза вызвано прямой передачей инфекции, ранняя диагностика и начало эффективной терапии в сочетании с эффективной профилактической терапией близких контактов должна стать ключевым приоритетом в профилактике этих состояний220-226. Кроме того, нужно обеспечить доступ к новым, лучше переносимым противотуберкулезным препаратам. Стратегии, которые прибегают к использованию этих лекарств только в качестве последнего средства, вероятно, приведут к увеличению лекарственной устойчивостии не являются ни научно обоснованными, ни персонализированными. Скорее, стратегии для реализации новых схем лечения туберкулеза должны учитывать факторы, которые привели ключевые препараты первого ряда к получению устойчивости. Такие факторы включают различную индивидуальную фармакокинетику, сопутствующие заболевания (особенно те, которые могут влиять на всасывание препаратов, например, ВИЧ), плохое качество лекарств, неадекватную дозировку, слабые цепочки поставок, а также неадекватное назначение препаратов и нерегулярное соблюдение схем лечения228–233. Слабые системы здравоохранения, которые предлагают неполную поддержку пациентам и их семьям, способствуют многим из этих факторам, подчеркивая важность их укрепления, чтобы помочь ликвидации эпидемии лекарственно-устойчивого туберкулеза и обеспечить более персонализированную медицинскую помощь234–236. Поскольку лекарственная устойчивость к туберкулезу возникает спонтанно и может появиться во время лечения237, использование стандартных комбинированных схем лечения пациентов с невыявленной лекарственной устойчивостью, вероятно, способствует дальнейшему приобретению устойчивости в дополнение к неблагоприятным исходам лечения пациентов238–243. В этом отношении решающее значение имеют надежные механизмы управления, особенно в частном секторе, например, описанные недавно для большой частной больницы в Индии244.
Расширение универсального доступа к быстрому тестированию на лекарственную чувствительность
Учитывая четкие требования по выявлению и лечению всех лиц с лекарственно-устойчивым туберкулезом и предотвращению появления лекарственной устойчивости в дальнейшем, ключевой рекомендацией данной Комиссии является применение универсального теста на лекарственную чувствительность (ТЛЧ) как минимум, к рифампицину, с доступностью лечения препаратами второй линии. Для пациентов, которые не отвечают на терапию препаратами первой линии, необходимо проводить скорейшее использование молекулярного ТЛЧ, чтобы исключить практику стандартизированной повторной терапии со схемами, включающими в себя только один дополнительный препарат и, скорее всего, способствующими усилению резистентности, в дополнение к слабым результатам лечения.
До относительно недавнего времени диагноз лекарственно-устойчивого туберкулеза основывался на исследовании культуры M. tuberculosis с последующей длительной отсрочкой диагностики и необходимостью в специализированных лабораториях245. Поскольку лекарственно-устойчивый туберкулез возникает вследствие резистентных мутаций в бактериальном геноме, новые тесты, такие как Xpert MTB/Тест RIF246 и метод, основанный на гибридизации ДНК с линейными зондами247, опираются на идентификацию мутаций, определяющих лекарственную устойчивость. Эти более быстрые тесты сократили время, необходимое для получения результатов от месяцев до часов, и, соответственно время246, 248, требуемое для начала лечения в различных условиях249,250, и в некоторых странах они стали широко использоваться. Более новые версии этих и подобных тестов, включая секвенирование всего генома, как ожидается, расширят ассортимент лекарств, которые можно протестировать, и уменьшат зависимость от специализированных лабораторий251–253. Улучшенные возможности диагностики по месту оказания медицинской помощи, осуществляемой в то же время, что и первоначальный визит в медицинское учреждение, существенно улучшат выявляемость случаев и уменьшат потери в ходе оказания сложной многоступенчатой диагностической и лечебной помощи5,254,255.
Улучшение лечения лекарственно-устойчивого туберкулеза
Высокое бремя МЛУ-ТБ или рифампицин-устойчивого туберкулеза и плохие результаты лечения пациентов с этими формами заболевания подчеркивают необходимость безопасных и эффективных, менее токсичных, более коротких и менее дорогостоящих схем лечения66,256–259. Обнадеживает, что стали доступны для использования два новых препарата (бедаквилин и деламанид) в лечении туберкулеза множественной лекарственной устойчивости или устойчивости к рифампицину260–262. Эти препараты наряду с лекарствами, перепрофилированными на лечение туберкулеза (включая линезолид и клофазимин) и претоманид (препарат, аналогичный деламаниду), включены в ряд новых, более коротких схем для орального применения, тестируемых в клинических испытаниях в отношении МЛУ-ТБ или рифампицин-резистентного туберкулеза263. Однако придется ждать несколько лет результатов большинства этих испытании264. Между тем, эти новые и перепрофилированные на лечение туберкулеза препараты все чаще используются в противотуберкулезных программах. Данные из ЮАР предполагают резкое улучшение показателей смертности и сокращение неэффективности лечения среди более 3000 пациентов, которых лечили бедаквилином265. Как прямой результат этих мероприятий, ЮАР объявила в 2018 году о внедрении безиньекционной бедаквилин-содержащей терапии для всех пациентов с рифампицин-резистентным туберкулезом266.
Данные по ЮАР, дополненные большим мета-анализом данных на каждого пациента с МЛУ-ТБ, легли в основу разработки нового руководства ВОЗ по определению приоритетности использования бедаквилина и линезолида267. Насколько нам известно, данных для аналогичного определения приоритетности использования для деламанида на сегодняшний день пока еще недостаточно. Увеличение использования этих новых и перепрофилированных на лечение туберкулеза лекарств поможет устранить зависимость от некоторых из наиболее токсичных и менее эффективных препаратов, включая инъекционные препараты второго ряда, использование которых чревато необратимой потерей слуха у 50% пациентов268. Это также поможет уменьшить нагрузку на систему здравоохранения по обеспечению ежедневных инъекций269. Однако, применение новых препаратов на основе предыдущих рекомендаций ВОЗ было ограничено, несмотря на дотации Агентства США по международному развитию (USAID) и компании Janssen Pharmaceuticals (Бирс, Бельгия) во многих странах270. Барьеры для использования этих препаратов включают затраты на лекарственные средства, трудности в получении разрешений от регулирующих органов и процедур закупок в отдельных странах, отсутствие государственной поддержки на высоком уровне271. Преодоление этих барьеров будет означать существенное движение вперед. Программы по туберкулезу также должны непрерывно развиваться, обеспечивая, чтобы руководящие принципы и клиническая практика опирались на лучшие имеющиеся доказательства, контроль за этим должны осуществлять организации гражданского общества.
Кроме того, более индивидуальный подход к лечению лекарственно-устойчивого туберкулеза, тот, который обеспечивает доступ ко всем препаратам второго ряда и руководствуется более обширным ТЛЧ путем секвенирования всего генома, позволит пациентам получать лучший шанс на выздоровление, одновременно ограничивая ненужное использование токсичных лекарств и усиление резистентности272. Такой подход должен подкрепляться внедрением исследований, чтобы интегрировать его в существующие программы борьбы с туберкулезом и систему здравоохранения в целом, в дополнение к системе фармаконадзора264,273,274. Хотя полностью индивидуальный подход к лечению трудно осуществить во всех ситуациях, потенциально возможно внедрение более стратифицированных подходов, учитывающих местные характеристики лекарственной устойчивости275.
Учитывая тяжелый характер имеющихся схем лечения туберкулеза (включая токсичность и длительность), а также социально-экономические проблемы, многие пациенты прекращают лечение, не дожидаясь завершения полного курса, доля таких пациентов по всему миру из данных когортного исследования, представленного в ВОЗ, составила 15%, и колеблется в пределах от 1% до 56% по данным отдельных исследований с тенденцией к увеличению66,276. Эти данные подчеркивают необходимость реализации подходов, более ориентированных на человека и семью, гарантирующих, что системы здравоохранения оптимально согласованы с потребностями населения, страдающего от лекарственно-устойчивого туберкулеза. Хотя упор был сделан на улучшение приверженности терапии и снижение огромных расходов, персонализированная модель оказания медицинской помощи также обеспечивает, чтобы пациенты с возможным лекарственно-устойчивым туберкулезом (и те, кто заботится о них) были полностью информированы о выборе метода терапии и других решениях в отношении лечения. Такие модели должны бороться с активной дискриминацией в системе здравоохранения и в других секторах. Персонализированная помощь также подразумевает предоставление лечения ближе к месту проживания пациентов и месту первоначального обращения за помощью (т.е. лечебные центры должны быть максимально децентрализованными и располагаться близко к пользователям) 277 . Полная реализация такого децентрализованного подхода требует значительного повышения мощности периферийных медицинских учреждений, чтобы вести пациентов со сложными характеристиками лекарственной резистентности, которым требуется индивидуальная терапия. Такие медицинские учреждения должны иметь легкодоступную, повседневную связь с центрами, назначившими лечение, и учреждениями, оказывающими экспертную высококвалифицированную помощь. Несмотря на возможное большое количество случаев лекарственно-устойчивого туберкулеза в стране или регионе, в совокупности на уровне периферийных медицинских учреждений таких пациентов может быть очень мало, но они могут появиться в любой момент времени. Поэтому ввиду нехватки опыта ведения таких пациентов децентрализацию необходимо внедрять наряду с обеспечением поддержки от экспертов, даже если они находятся на удаленном расстоянии.
Предупреждение развития лекарственной резистентности
Хотя диагностика и безотлагательное лечение имеют решающее значение для борьбы с эпидемией туберкулеза, первостепенное значение также имеет минимизация риска дальнейшего развития лекарственной резистентности как к существующим препаратам первой линии, так и к препаратам второго ряда и новым лекарственным средствам. Снижение распространения лекарственно-устойчивого туберкулеза включает устранение ведущих факторов развития лекарственной резистентности туберкулеза посредством улучшения качества программ, равно как и отказ от использования стандартизированных схем при отсутствии ТЛЧ при каждом возможном случае. Наконец, рациональное использование антибиотиков гарантирует, что новые лекарства будут использоваться в специально подобранных, эффективных схемах лечения для всех пациентов с лекарственно-устойчивым туберкулезом, а не только при ограниченных возможностях лечения. Такой подход должен также поддерживаться усиленным надзором за лекарственно-устойчивым туберкулезом (заменяя эпизодические, дорогостоящие исследования лекарственно-устойчивого туберкулеза).
Как и в случае лекарственно-чувствительного туберкулеза, лечение скрытого лекарственно-устойчивого туберкулеза может существенно повлиять на эпидемию в долгосрочной перспективе. Как минимум два клинических испытания оценивают сейчас различные схемы профилактики для лиц, находящихся в тесном контакте с пациентами с МЛУ-ТБ или с рифампицин-резистентным туберкулезом263. Кроме того, в 2018 году ВОЗ выпустила условную рекомендацию, поддерживающую использование индивидуального профилактического лечения контактов таких пациентов, которые подвержены высокому риску заболевания 278. Учитывая высокую заболеваемость и смертность, связанные с лекарственно-устойчивым туберкулезом, приоритетом является профилактическое лечение таких групп высокого риска, включая детей, а также людей, инфицированных ВИЧ
Увеличение распространенности лекарственно-устойчивого туберкулеза как угроза безопасности для глобального здоровья — последствия для донорского финансирования
Стоимость лечения для пациентов с МЛУ-ТБ или рифампицин-устойчивым туберкулезом варьирует по оценкам от 1218 долларов США в странах с низким уровнем доходов до 83365 долларов США в странах с высоким уровнем доходов279. До сегодняшнего дня высокая стоимость была большим препятствием для лечения в широких масштабах. Партнерство «Остановить туберкулез» оценило, что в 2017 году для финансирования помощи, оказываемой для программ по лекарственно-устойчивому туберкулезу, потребовалось 2 млрд. долл. США; ожидается увеличение этих расходов до 3–6 млрд. долларов США к 2020 году66. И эти суммы вряд ли останутся на этом уровне для многих стран с высоким бременем МЛУ-ТБ или рифампицин-устойчивого туберкулеза; страны БРИКС (Бразилия, Россия, Индия, Китай и Южная Африка) являются заметными исключениями. Как следствие, вероятно, потребуется финансирование для поддержки реализации программы в области лекарственной устойчивости, от международных источников, даже в странах, имеющих возможность финансировать свои собственные программы. Существующие и будущие прогнозируемые экономические затраты, связанные с лекарственно-устойчивым туберкулезом, обеспечивают убедительные обоснования для увеличения донорского финансирования, даже для стран со средним уровнем доходов, считающихся выходящими из категории получателей донорской помощи280,281.